
Neuroimaging-유성혜 교수
Neurointervention-백성현 교수
Thoracic Imaging-황성호 교수
Cardiovascular Imaging-이종민 교수
Breast Imaging-김민정 교수
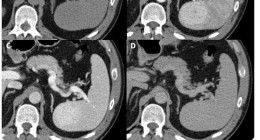
Abdominal Imaging-이승수 교수
Abdominal Imaging-강효진 교수
Urogenital Imaging-나성은 교수, 김승협 명예교수
Intervention-권동일 교수
Musculoskeletal Imaging-차장규 교수
Pediatric Imaging-이미정 교수
2025 7월 국제학회일정
2025 8월 국제학회일정
2025 9월 국제학회일정
| SUN | MON | TUE | WED | THU | FRI | SAT |
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | |
| 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 21 | 22 | 23 | 24 | 25 | 26 | 27 |
| 28 | 29 | 30 |
| 일정제목 | 날짜 |
| ASHNR 2024 (American Society of Head and Neck Radiology) | 09/04/2024 ~ 09/08/2024 |
| ASCI 2024 (Asian Society of Cardiovascular Imaging) | 09/12/2024 ~ 09/14/2024 |
| CIRSE 2024 (Cardiovascular and Interventional Radiological Society of Europe) | 09/14/2024 ~ 09/18/2024 |
| ESNR 2024 (European Society of Neuroradiology) | 09/18/2024 ~ 09/22/2024 |
| NASCI 2024 (North American Society for Cardiovascular Imaging) | 09/21/2024 ~ 09/24/2024 |
| ASER 2024 (American Society of Emergency Radiology | 09/11/2024 ~ 09/14/2024 |
| ASHNR 2024 (American Society of Head and Neck Radiology | 09/04/2024 ~ 09/09/2024 |
| ASCI 2024 (Asian Society of Cardiovascular Imaging) | 09/12/2024 ~ 09/14/2024 |
| CIRSE 2024 (Cardiovascular and Interventional Radiological Society of Europe) | 09/14/2024 ~ 09/18/2024 |
| ISS 2024 (International Skeletal Society) | 09/15/2024 ~ 09/20/2024 |
| ESNR 2024 (European Society of Neuroradiology) | 09/18/2024 ~ 09/22/2024 |
| ESUR 2024 (European Society of Urogenital Radiology | 09/19/2024 ~ 09/22/2024 |
| NASCI 2024 (North American Society for Cardiovascular Imaging) | 09/21/2024 ~ 09/24/2024 |
| AOSPR 2024 (Asian and Oceanic Society for Pediatric Radiology | 09/25/2024 ~ 09/28/2024 |
| ASHNR 2024 (American Society of Head and Neck Radiology) | 09/04/2024 ~ 09/08/2024 |
| ASCI 2024 (Asian Society of Cardiovascular Imaging) | 09/12/2024 ~ 09/14/2024 |
| CIRSE 2024 (Cardiovascular and Interventional Radiological Society of Europe) | 09/14/2024 ~ 09/18/2024 |
| ISS 2024 (International Skeletal Society) | 09/15/2024 ~ 09/20/2024 |
| ESNR 2024 (European Society of Neuroradiology) | 09/18/2024 ~ 09/22/2024 |
| ESUR 2024 (European Society of Urogenital Radiology) | 09/19/2024 ~ 09/22/2024 |
| NASCI 2024 (North American Society for Cardiovascular Imaging) | 09/21/2024 ~ 09/24/2024 |
| AOSPR 2024 (Asian and Oceanic Society for Pediatric Radiology) | 09/25/2024 ~ 09/28/2024 |

 서울시 강남구 논현로72길 29, 3층 메디칼업저버 / TEL : 02) 3467-5482
서울시 강남구 논현로72길 29, 3층 메디칼업저버 / TEL : 02) 3467-5482
Copyright © Radiology Digest All rights reserved.
